Автор:
Christy White
Жаратылган Күнү:
8 Май 2021
Жаңыртуу Күнү:
1 Июль 2024

Мазмун
- Басуу
- 3-ыкманын 1-ыкмасы: Биринчи бөлүк: Электрондордун кабыктарын түшүнүү
- 3-ыкманын 2-ыкмасы: Экинчи бөлүк: Өткөөл металлдардан башка металлдарда валенттүүлүк электронун табуу
- 3-ыкманын 3-ыкмасы: Үчүнчү бөлүк: Өткөөл металлдарда валенттүүлүк электрондорун табуу
- Сунуштар
- Зарылчылыктар
Валенттик электрондор элементтин сырткы кабыгында жатат. Атомдогу валенттүүлүк электрондорунун саны бул элементтин пайда боло турган химиялык байланыш түрүн аныктайт. Валенттик электрондордун санын билүүнүн эң жакшы жолу - бул элементтердин мезгилдик системасын колдонуу.
Басуу
3-ыкманын 1-ыкмасы: Биринчи бөлүк: Электрондордун кабыктарын түшүнүү
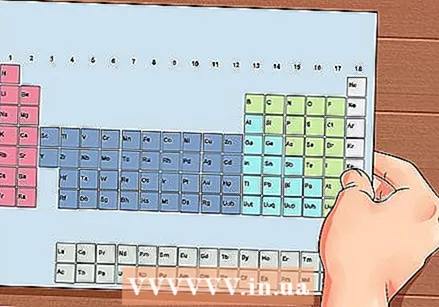 Элементтердин мезгилдик системасы. Бул түстүү коддору бар таблица, анда ар бир уячада бир элемент атом номери жана 1ден 3кө чейин тамга менен символ катары көрсөтүлөт.
Элементтердин мезгилдик системасы. Бул түстүү коддору бар таблица, анда ар бир уячада бир элемент атом номери жана 1ден 3кө чейин тамга менен символ катары көрсөтүлөт. 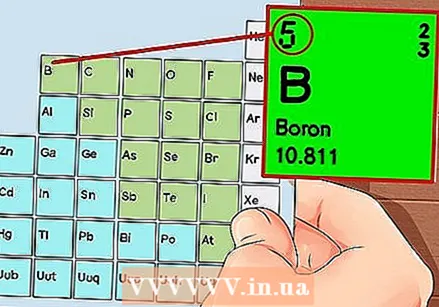 Элементтин атомдук номерин тап. Атом номери элементтин белгисинин үстүндө же жанында. Мисалы: Бор (В) атомдук саны 5ке ээ, демек, анын 5 протон жана 5 электрон бар.
Элементтин атомдук номерин тап. Атом номери элементтин белгисинин үстүндө же жанында. Мисалы: Бор (В) атомдук саны 5ке ээ, демек, анын 5 протон жана 5 электрон бар. 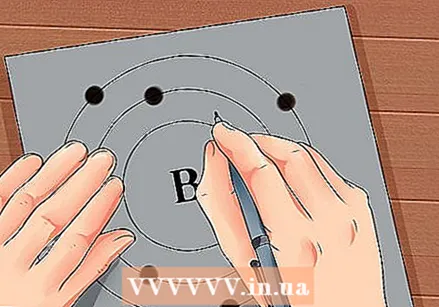 Атомдун жөнөкөй сүрөтүн тартыңыз жана электрондорду ядронун айланасындагы орбитага жайгаштырыңыз. Бул жумуштар снаряд же энергия деңгээли деп да аталат. Бир эле кабыкта болушу мүмкүн болгон электрондордун максималдуу саны белгиленип, кабыктар ички орбитага чейин толтурулат.
Атомдун жөнөкөй сүрөтүн тартыңыз жана электрондорду ядронун айланасындагы орбитага жайгаштырыңыз. Бул жумуштар снаряд же энергия деңгээли деп да аталат. Бир эле кабыкта болушу мүмкүн болгон электрондордун максималдуу саны белгиленип, кабыктар ички орбитага чейин толтурулат. - K Shell (ички): максимум 2 электрон.
- L Shell: максимум 8 электрон.
- М Shell: максимум 18 электрон.
- N Shell: максимум 32 электрон.
- O Shell: максимум 50 электрон.
- P Shell (тышкы): максимум 72 электрон.
 Сырткы катмардагы электрондордун санын табыңыз. Бул валенттик электрондор.
Сырткы катмардагы электрондордун санын табыңыз. Бул валенттик электрондор. - Валенттик кабык толгондо, элемент туруктуу болот.
- Эгерде валенттик кабык толук эмес болсо, анда элемент реактивдүү болот, демек, ал башка элементтин атому менен химиялык байланышта болот. Ар бир атом валенттүүлүк электрондорун бөлүшүп, валенттик кабыгын толтурууга аракет кылат.
3-ыкманын 2-ыкмасы: Экинчи бөлүк: Өткөөл металлдардан башка металлдарда валенттүүлүк электронун табуу
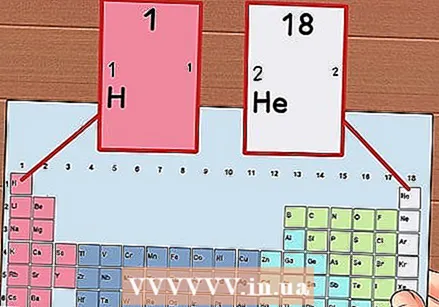 Мезгилдик таблицанын ар бир тилкесин 1ден 18ге чейин номерлеңиз. Суутек (H) 1-графанын башында, Гелий (He) 18-графанын үстүндө жайгашкан. Бул элементтердин ар кандай топтору.
Мезгилдик таблицанын ар бир тилкесин 1ден 18ге чейин номерлеңиз. Суутек (H) 1-графанын башында, Гелий (He) 18-графанын үстүндө жайгашкан. Бул элементтердин ар кандай топтору. 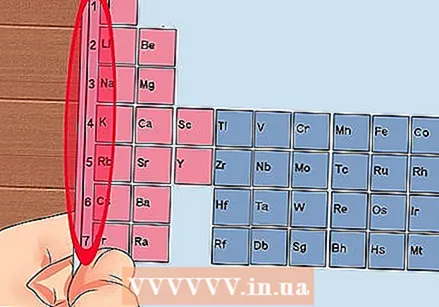 Ар бир катарга 1ден 7ге чейин номер бериңиз. Бул элементтердин периоддору жана алар атомдордун кабыкчаларына же энергетикалык деңгээлдерине туура келет.
Ар бир катарга 1ден 7ге чейин номер бериңиз. Бул элементтердин периоддору жана алар атомдордун кабыкчаларына же энергетикалык деңгээлдерине туура келет. - Суутектин (Н) жана Гелийдин (Ал) экиден кабыгы 1ден, ал эми Франций (Фр) 7ден турат.
- Лантаноиддер жана актиниддер топтолуп, негизги таблицанын ылдый жагында келтирилген. Бардык лантаноиддер 6-мезгил, 3-топко жана бардык актиниддер 7-мезгил, 3-топко таандык.
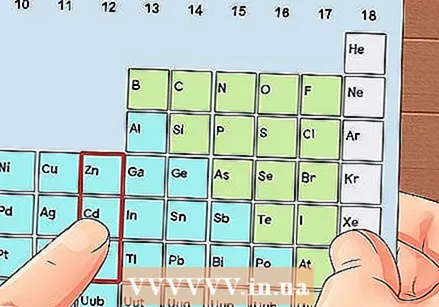 Өткөөл металл болбогон элементти табыңыз. Өтмө металлдар 3төн 12ге чейинки топтордо, калган металлдардын топтук номерлери валенттүүлүк электрондорунун санын көрсөтөт.
Өткөөл металл болбогон элементти табыңыз. Өтмө металлдар 3төн 12ге чейинки топтордо, калган металлдардын топтук номерлери валенттүүлүк электрондорунун санын көрсөтөт. - 1-топ: 1 валенттик электрон
- 2-топ: 2 валенттик электрондор
- 13-топ: 3 валенттик электрондор
- 14-топ: 4 валенттик электрондор
- 15-топ: 5 валенттик электрондор
- 16-топ: 6 валенттик электрондор
- 17-топ: 7 валенттик электрондор
- 18-топ: 8 валенттик электрондор - Гелийден башка, анда 2
3-ыкманын 3-ыкмасы: Үчүнчү бөлүк: Өткөөл металлдарда валенттүүлүк электрондорун табуу
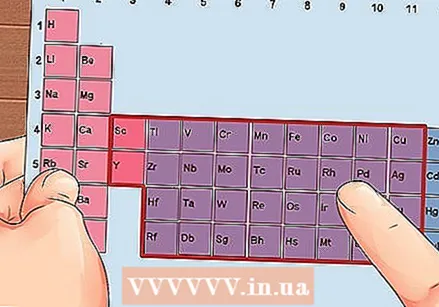 3төн 12ге чейинки топтогу элементти, өткөөл металлдарды табыңыз.
3төн 12ге чейинки топтогу элементти, өткөөл металлдарды табыңыз. Топтун номерине таянып, валенттик электрондордун санын аныктаңыз. Бул топтун сандары валенттүүлүк электрондорунун мүмкүн болгон санына туура келет.
Топтун номерине таянып, валенттик электрондордун санын аныктаңыз. Бул топтун сандары валенттүүлүк электрондорунун мүмкүн болгон санына туура келет. - 3-топ: 3 валенттик электрондор
- 4-топ: 2ден 4кө чейин валенттик электрондор
- 5-топ: 2ден 5ке чейин валенттик электрондор
- 6-топ: 2ден 6га чейин валенттик электрондор
- 7-топ: 2ден 7ге чейин валенттик электрондор
- 8-топ: 2 же 3 валенттик электрондор
- 9-топ: 2 же 3 валенттик электрондор
- 10-топ: 2 же 3 валенттик электрондор
- 11-топ: 1 же 2 валенттик электрондор
- 12-топ: 2 валенттик электрондор
Сунуштар
- Өтмө металлдарда валенттик кабыктар болушу мүмкүн, алар толугу менен толук эмес. Өтмө металлдардагы валенттүүлүк электрондорунун так санын аныктоо үчүн кванттык теориянын белгилүү бир принциптери талап кылынат, алар бул макаладан тышкары.
Зарылчылыктар
- Элементтердин мезгилдик системасы
- Карандаш
- Кагаз