Автор:
Bobbie Johnson
Жаратылган Күнү:
10 Апрель 2021
Жаңыртуу Күнү:
1 Июль 2024
Мазмун
- Кадамдар
- 2 ичинен 1 -бөлүк: Жабдууларды даярдоо
- 2 ичинен 2 -бөлүк: Эксперимент жүргүзүү
- Кеңештер
- Эскертүүлөр
- Сага эмне керек
Суу бөлүү процесси (H2O) электр энергиясын колдонуу менен анын курамына (суутек жана кычкылтек) электролиз деп аталат. Электролиздин натыйжасында алынган газдар өз алдынча колдонулушу мүмкүн - мисалы, суутек эң таза энергия булактарынын бири катары кызмат кылат. Бул процесстин аталышы бир аз акылдуу угулушу мүмкүн, бирок, эгерде сизде керектүү жабдуулар, билимдер жана бир аз тажрыйба болсо, бул көрүнгөндөн да оңой.
Кадамдар
2 ичинен 1 -бөлүк: Жабдууларды даярдоо
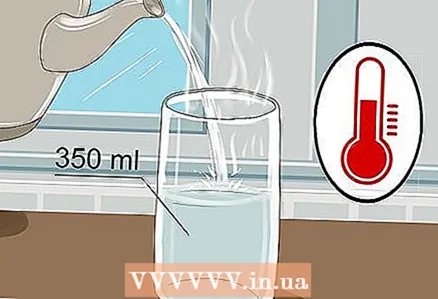 1 350 мл стаканды алып, ичине жылуу суу куюңуз. Стаканды аягына чейин толтуруунун кереги жок, бир аз суу жетиштүү. Муздак суу болот, бирок жылуу суу электр энергиясын жакшы өткөрөт.
1 350 мл стаканды алып, ичине жылуу суу куюңуз. Стаканды аягына чейин толтуруунун кереги жок, бир аз суу жетиштүү. Муздак суу болот, бирок жылуу суу электр энергиясын жакшы өткөрөт. - Кран суусу да, бөтөлкөдөгү суу да жасайт.
- Жылуу суунун илешкектүүлүгү төмөн болгондуктан, иондордун айланышын жеңилдетет.
 2 1 аш кашык (20 грамм) ашкана тузун сууга эритип алыңыз. Стаканга туз куюп, сууну ээритүү үчүн аралаштырыңыз. Бул туздуу эритмени түзөт.
2 1 аш кашык (20 грамм) ашкана тузун сууга эритип алыңыз. Стаканга туз куюп, сууну ээритүү үчүн аралаштырыңыз. Бул туздуу эритмени түзөт. - Натрий хлориди (б.а. туз тузу) - суунун электр өткөрүмдүүлүгүн жогорулатуучу электролит. Суу өзү эле электр энергиясын жакшы өткөрбөйт.
- Суунун электр өткөрүмдүүлүгүн жогорулаткандан кийин, батарея жараткан ток эритмеден оңой өтөт жана молекулаларды суутек менен кычкылтекке эффективдүү бөлөт.
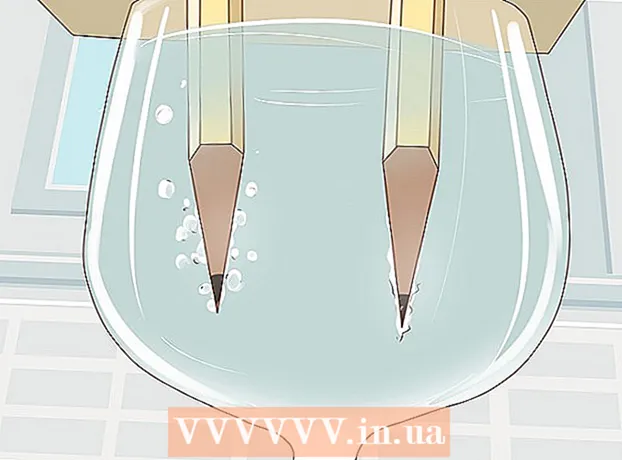
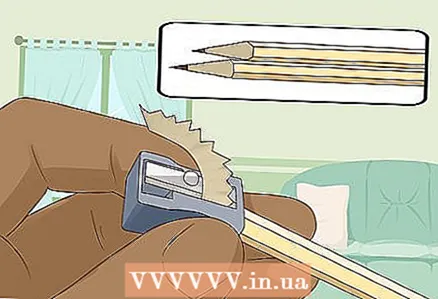 3 Коргошунду ачуу үчүн эки учунда эки катуу жумшак карандашты курчутуңуз. Карандаштарыңыздан өчүргүчтү алып салууну унутпаңыз. Графит таягы эки учунда тең чыгып турушу керек.
3 Коргошунду ачуу үчүн эки учунда эки катуу жумшак карандашты курчутуңуз. Карандаштарыңыздан өчүргүчтү алып салууну унутпаңыз. Графит таягы эки учунда тең чыгып турушу керек. - Графит таякчалары сиз батареяны туташтырган изоляцияланган электрод катары кызмат кылат.
- Графит бул экспериментке абдан ылайыктуу, анткени ал сууда ээрибейт жана дат баспайт.
 4 Айнектин үстүнө жаткандай чоң картон баракчасын кесип алыңыз. Картонду колдонуңуз, анын ичине эки тешикти салгандан кийин салбырап калбайт. Бут кийим кутусунан же окшошунан төрт бурчтуу кесимди кесип алыңыз.
4 Айнектин үстүнө жаткандай чоң картон баракчасын кесип алыңыз. Картонду колдонуңуз, анын ичине эки тешикти салгандан кийин салбырап калбайт. Бут кийим кутусунан же окшошунан төрт бурчтуу кесимди кесип алыңыз. - Картон карандашты стакандын капталына жана түбүнө тийбеши үчүн сууда кармоо үчүн колдонулат.
- Картон өткөргүч эмес, андыктан аны стаканга коопсуз коюңуз.
 5 Карандаш менен картон менен эки тешикти чукуңуз. Картонду карандаш менен тешиңиз - бул учурда алар бекем кысылып, тайып кетпейт. Графит айнектин капталына же түбүнө тийбешин текшериңиз, антпесе экспериментке тоскоол болот.
5 Карандаш менен картон менен эки тешикти чукуңуз. Картонду карандаш менен тешиңиз - бул учурда алар бекем кысылып, тайып кетпейт. Графит айнектин капталына же түбүнө тийбешин текшериңиз, антпесе экспериментке тоскоол болот.
2 ичинен 2 -бөлүк: Эксперимент жүргүзүү
 1 Ар бир батарея терминалына аллигатор клиптери бар бир зымды туташтырыңыз. Батарея электр тогунун булагы катары кызмат кылат жана кыскычтары жана графит таякчалары бар зымдар аркылуу ток сууга жетет.Кыскыч менен бир зымды позитивге, экинчисин батарейканын терс терминалына туташтырыңыз.
1 Ар бир батарея терминалына аллигатор клиптери бар бир зымды туташтырыңыз. Батарея электр тогунун булагы катары кызмат кылат жана кыскычтары жана графит таякчалары бар зымдар аркылуу ток сууга жетет.Кыскыч менен бир зымды позитивге, экинчисин батарейканын терс терминалына туташтырыңыз. - 6 вольттуу батареяны колдонуңуз. Эгерде сизде жок болсо, анын ордуна 9 вольттуу батареяны колдонсоңуз болот.
- Ылайыктуу батареяны электр менен камсыздоо дүкөнүнөн же супермаркеттен алсаңыз болот.
 2 Зымдардын башка учтарын карандаштарга туташтырыңыз. Металл зымдын кыскычтарын графит таякчаларына бекем бекиткиле. Клиптердин графит таякчаларынан тайып кетпеши үчүн, карандаштан дагы бир нече жыгачты тазалоо керек болушу мүмкүн.
2 Зымдардын башка учтарын карандаштарга туташтырыңыз. Металл зымдын кыскычтарын графит таякчаларына бекем бекиткиле. Клиптердин графит таякчаларынан тайып кетпеши үчүн, карандаштан дагы бир нече жыгачты тазалоо керек болушу мүмкүн. - Ошентип, сиз схеманы жабасыз, ал эми батареядан ток суу аркылуу өтөт.
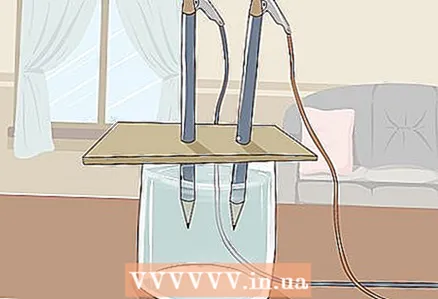 3 Картонду карандаштардын бош учтары сууга чөгүп кетиши үчүн айнекке кой. Картон баракчасы айнектин үстүндө эс алгыдай чоң болушу керек. Карандаштарды туура жайгаштырууну бузбоо үчүн этият болуңуз.
3 Картонду карандаштардын бош учтары сууга чөгүп кетиши үчүн айнекке кой. Картон баракчасы айнектин үстүндө эс алгыдай чоң болушу керек. Карандаштарды туура жайгаштырууну бузбоо үчүн этият болуңуз. - Эксперимент ийгиликтүү болушу үчүн графит айнектин дубалдарына жана түбүнө тийбеши керек. Муну дагы бир жолу текшериңиз жана керек болсо карандаштарды тууралаңыз.
 4 Суунун суутек менен кычкылтекке бөлүнүшүн караңыз. Сууга чөмүлгөн графит таякчаларынан газ көбүктөрү көтөрүлө баштайт. Бул суутек жана кычкылтек. Водород терс уюлда, кычкылтек оң уюлда бөлүнүп чыгат.
4 Суунун суутек менен кычкылтекке бөлүнүшүн караңыз. Сууга чөмүлгөн графит таякчаларынан газ көбүктөрү көтөрүлө баштайт. Бул суутек жана кычкылтек. Водород терс уюлда, кычкылтек оң уюлда бөлүнүп чыгат. - Зымдарды аккумуляторго жана графит таякчаларына туташтыраар замат суу аркылуу электр тогу өтөт.
- Терс полюска туташкан карандашта дагы газдын көбүктөрү пайда болот, анткени ар бир суу молекуласы эки суутек атомунан жана бир кычкылтек атомунан турат.
Кеңештер
- Эгерде сизде графит шахталары бар карандаштар жок болсо, анын ордуна эки кичинекей зымды колдонсоңуз болот. Жөн эле ар бир зымдын бир учун батареянын тиешелүү мамысына ороп, экинчисин сууга малып коюңуз. Натыйжа карандаш менен бирдей болот.
- Башка батареяны колдонуп көрүңүз. Аккан токтун көлөмү батареянын чыңалуусуна көз каранды, бул өз кезегинде суу молекулаларынын бөлүнүү ылдамдыгына таасир этет.
Эскертүүлөр
- Эгерде сиз сууга туз сыяктуу электролит кошсоңуз, анда эксперимент хлор сыяктуу кошумча продукттун аз өлчөмүн пайда кылаарын унутпаңыз. Бул аз өлчөмдө коопсуз, бирок бир аз хлордун жытын сезе аласыз.
- Бул экспериментти чоңдордун көзөмөлү астында аткарыңыз. Бул электр энергиясы жана газдар менен байланышкан жана андыктан коркунучтуу болушу мүмкүн.
Сага эмне керек
- Эки катуу карандаш
- Бир 6 же 9 вольттуу батарея
- Көлөмү 350 миллилитр болгон айнек
- 2 зым крокодил клиптер менен
- Карандаш үчүн курчутуучу
- Туз