Автор:
Eric Farmer
Жаратылган Күнү:
10 Март 2021
Жаңыртуу Күнү:
1 Июль 2024
Мазмун
- Кадамдар
- Метод 1 2: Атомдордогу нейтрондордун санын аныктоо (изотоптор эмес)
- Метод 2 2: Изотоптордогу нейтрондордун санын аныктоо
- Кеңештер
Ошол эле элементтин атомдорунда протондордун саны туруктуу, ал эми нейтрондордун саны ар кандай болушу мүмкүн.Белгилүү бир атомдо канча нейтрон бар экенин билүү менен, ал кадимки атомбу же аз же көп нейтронго ээ болгон изотоп экенин аныктай аласыз. Атомдогу нейтрондордун санын аныктоо өтө жөнөкөй. Атомдогу же изотоптогу нейтрондордун санын эсептөө үчүн биздин көрсөтмөлөрдү аткаруу жана мезгилдик таблицаны колдо кармоо гана керек.
Кадамдар
Метод 1 2: Атомдордогу нейтрондордун санын аныктоо (изотоптор эмес)
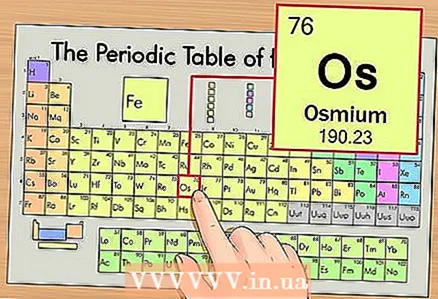 1 Мезгилдик таблицадан элементти табыңыз. Мисал катары, биз алтынчы мезгилде (жогорудан алтынчы катар) турган осмийди (Ос) карап чыгабыз.
1 Мезгилдик таблицадан элементти табыңыз. Мисал катары, биз алтынчы мезгилде (жогорудан алтынчы катар) турган осмийди (Ос) карап чыгабыз.  2 Элементтин атомдук номерин табыңыз. Бул, эреже катары, элементтин уячасындагы эң көрүнүктүү сан жана адатта анын символунун үстүндө жайгашкан (биздин мисалда колдонгон мезгилдик таблицанын версиясында башка сандар жок). Атомдук сан - бул элементтин бир атомундагы протондордун саны. Осмий үчүн бул сан 76, башкача айтканда, бир осмий атомунда 76 протон бар.
2 Элементтин атомдук номерин табыңыз. Бул, эреже катары, элементтин уячасындагы эң көрүнүктүү сан жана адатта анын символунун үстүндө жайгашкан (биздин мисалда колдонгон мезгилдик таблицанын версиясында башка сандар жок). Атомдук сан - бул элементтин бир атомундагы протондордун саны. Осмий үчүн бул сан 76, башкача айтканда, бир осмий атомунда 76 протон бар. - Протондордун саны өзгөрүүсүз, бул элементти элемент кылат.
 3 Элементтин атомдук массасын табыңыз. Бул сан көбүнчө элементтин символунун астынан табылат. Биздин мисалда мезгилдик системанын версиясында атомдук масса берилбегенине көңүл бургула (бул дайыма эле боло бербейт; мезгилдик системанын көптөгөн версияларында атомдук масса көрсөтүлгөн). Осмийдин атомдук массасы 190.23.
3 Элементтин атомдук массасын табыңыз. Бул сан көбүнчө элементтин символунун астынан табылат. Биздин мисалда мезгилдик системанын версиясында атомдук масса берилбегенине көңүл бургула (бул дайыма эле боло бербейт; мезгилдик системанын көптөгөн версияларында атомдук масса көрсөтүлгөн). Осмийдин атомдук массасы 190.23.  4 Атомдук массаны эң жакын бүтүн санга тегеректеңиз. Биздин мисалда, 190.23 190га чейин тегеректелген.
4 Атомдук массаны эң жакын бүтүн санга тегеректеңиз. Биздин мисалда, 190.23 190га чейин тегеректелген. - Атомдук масса - бул белгилүү бир элементтин изотопторунун орточо саны, адатта ал бүтүн сан катары көрсөтүлбөйт.
 5 Атомдук массадан атомдук номурду алып салуу. Протондор менен нейтрондор атомдук массанын абсолюттук бөлүгүн түзгөндүктөн, атомдук массадан протондордун санын (башкача айтканда, протондордун санына барабар болгон атомдук номурду) алып салуу атомдогу нейтрондордун санын берет. Ондук чекиттен кийинки сандар атомдогу өтө кичинекей электрон массасын билдирет. Биздин мисалда: 190 (атомдук салмагы) - 76 (протондордун саны) = 114 (нейтрондордун саны).
5 Атомдук массадан атомдук номурду алып салуу. Протондор менен нейтрондор атомдук массанын абсолюттук бөлүгүн түзгөндүктөн, атомдук массадан протондордун санын (башкача айтканда, протондордун санына барабар болгон атомдук номурду) алып салуу атомдогу нейтрондордун санын берет. Ондук чекиттен кийинки сандар атомдогу өтө кичинекей электрон массасын билдирет. Биздин мисалда: 190 (атомдук салмагы) - 76 (протондордун саны) = 114 (нейтрондордун саны). 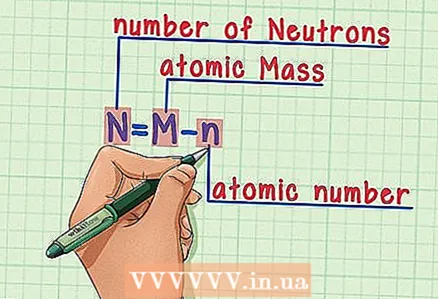 6 Формуланы унутпаңыз. Келечекте нейтрондордун санын табуу үчүн бул формуланы колдонуңуз:
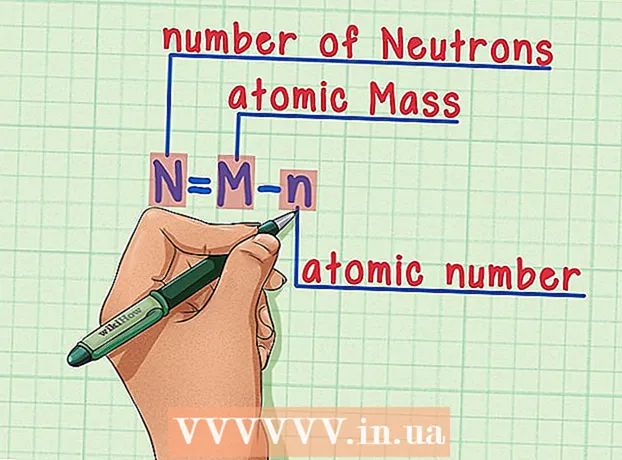
6 Формуланы унутпаңыз. Келечекте нейтрондордун санын табуу үчүн бул формуланы колдонуңуз: - N = M - n
- N = нейтрондордун саны
- M = атомдук массасы
- n = атомдук номер
- N = M - n
Метод 2 2: Изотоптордогу нейтрондордун санын аныктоо
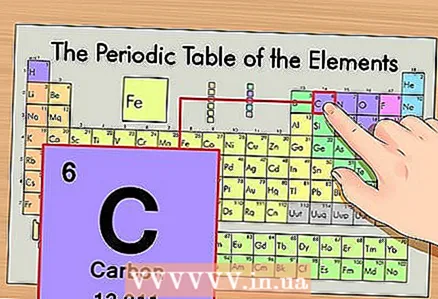 1 Мезгилдик таблицадан элементти табыңыз. Мисал катары, көмүртектин 14С изотопун карайбыз. Изотоптук эмес көмүртек 14C жөн эле көмүртек С болгондуктан, мезгилдүү таблицадан көмүрдү табыңыз (экинчи период же жогору жактан экинчи катар).
1 Мезгилдик таблицадан элементти табыңыз. Мисал катары, көмүртектин 14С изотопун карайбыз. Изотоптук эмес көмүртек 14C жөн эле көмүртек С болгондуктан, мезгилдүү таблицадан көмүрдү табыңыз (экинчи период же жогору жактан экинчи катар). 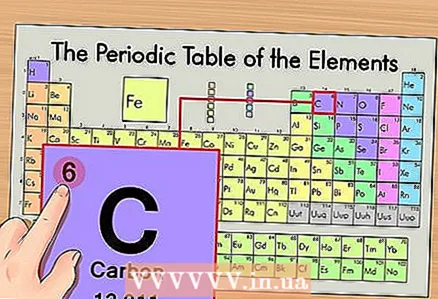 2 Элементтин атомдук номерин табыңыз. Бул, эреже катары, элементтин уячасындагы эң көрүнүктүү сан жана адатта анын символунун үстүндө жайгашкан (биздин мисалда колдонгон мезгилдик таблицанын версиясында башка сандар жок). Атомдук сан - бул элементтин бир атомундагы протондордун саны. Көмүр 6 саны, башкача айтканда, бир көмүрдүн алты протону бар.
2 Элементтин атомдук номерин табыңыз. Бул, эреже катары, элементтин уячасындагы эң көрүнүктүү сан жана адатта анын символунун үстүндө жайгашкан (биздин мисалда колдонгон мезгилдик таблицанын версиясында башка сандар жок). Атомдук сан - бул элементтин бир атомундагы протондордун саны. Көмүр 6 саны, башкача айтканда, бир көмүрдүн алты протону бар. 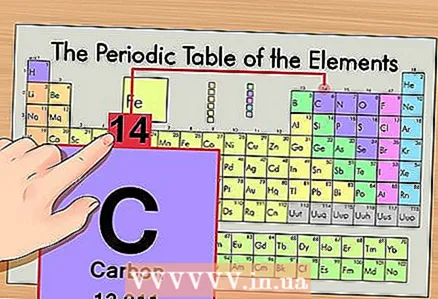 3 Атомдук массаны табыңыз. Изотоптор үчүн, муну кылуу абдан оңой, анткени алар атомдук массасына жараша аталышкан. Биздин учурда, көмүртек 14С атомдук массасы 14кө ээ. Эми биз изотоптун атомдук массасын билебиз; кийинки эсептөө процесси атомдордогу нейтрондордун санын аныктоо менен бирдей (изотоптор эмес).
3 Атомдук массаны табыңыз. Изотоптор үчүн, муну кылуу абдан оңой, анткени алар атомдук массасына жараша аталышкан. Биздин учурда, көмүртек 14С атомдук массасы 14кө ээ. Эми биз изотоптун атомдук массасын билебиз; кийинки эсептөө процесси атомдордогу нейтрондордун санын аныктоо менен бирдей (изотоптор эмес).  4 Атомдук массадан атомдук номурду алып салуу. Протондор менен нейтрондор атомдук массанын абсолюттук бөлүгүн түзгөндүктөн, атомдук массадан протондордун санын (башкача айтканда, протондордун санына барабар болгон атомдук номурду) алып салуу атомдогу нейтрондордун санын берет. Биздин мисалда: 14 (атомдук массасы) - 6 (протондордун саны) = 8 (нейтрондордун саны).
4 Атомдук массадан атомдук номурду алып салуу. Протондор менен нейтрондор атомдук массанын абсолюттук бөлүгүн түзгөндүктөн, атомдук массадан протондордун санын (башкача айтканда, протондордун санына барабар болгон атомдук номурду) алып салуу атомдогу нейтрондордун санын берет. Биздин мисалда: 14 (атомдук массасы) - 6 (протондордун саны) = 8 (нейтрондордун саны). 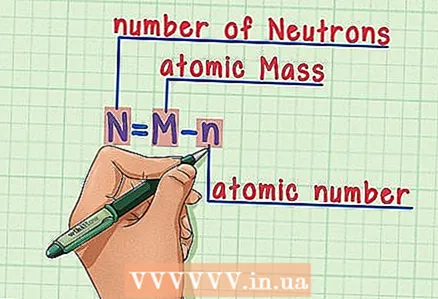 5 Формуланы унутпаңыз. Келечекте нейтрондордун санын табуу үчүн бул формуланы колдонуңуз:
5 Формуланы унутпаңыз. Келечекте нейтрондордун санын табуу үчүн бул формуланы колдонуңуз: - N = M - n
- N = нейтрондордун саны
- M = атомдук массасы
- n = атомдук номер
- N = M - n
Кеңештер
- Протондор менен нейтрондор элементтердин дээрлик абсолюттук массасын түзөт, ал эми электрондор жана башка бөлүкчөлөр өтө аз массаны түзөт (бул масса нөлгө жакын).Бир протондун массасы бир нейтрон менен бирдей болгондуктан жана атомдук саны протондордун саны болгондуктан, сиз жалпы массадан протондордун санын алып салсаңыз болот.
- Осмий - бөлмө температурасында катуу абалдагы металл, гректин "osme" - жыт деген сөзүнөн алынган.
- Эгерде сиз мезгилдик таблицада сан эмнени билдирерин билбесеңиз, эсиңизде болсун: стол адатта 1ден (суутектен) башталып, бир бирдикти солдон оңго карай өстүргөн атомдук номердин (башкача айтканда, протондордун саны) айланасында курулат. , 118 менен бүтөт (Oganesson). Себеби, атомдогу протондордун саны элементтин өзүн аныктайт жана мындай сан элементтерди уюштуруунун эң оңой жолу (мисалы, 2 протону бар атом дайыма гелий болот, 79 протону бар атом дайыма алтын болгондой эле) ).



