Автор:
Clyde Lopez
Жаратылган Күнү:
26 Июль 2021
Жаңыртуу Күнү:
1 Июль 2024

Мазмун
- Кадамдар
- Метод 1дин 4: Салмагы / Көлөмү Формуласын Пайыз менен Эсептөө
- Метод 2 4: Молекулярдык эритмени даярдоо
- Метод 3 3: Белгилүү концентрациядагы эритмелерди суюлтуу
- Метод 4 4: Коопсуздук чараларын сактоо
- Кеңештер
- Эскертүүлөр
- Сага эмне керек
Жөнөкөй химиялык эритмелерди үйдө же жумушта оңой эле ар кандай жолдор менен даярдаса болот. Сиз порошок материалдан чечим чыгарасызбы же суюктукту суюлтасызбы, ар бир компоненттин туура өлчөмүн аныктоо оңой. Химиялык эритмелерди даярдап жатканда, зыян келтирбөө үчүн жеке коргонуу каражаттарын колдонууну унутпаңыз.
Кадамдар
Метод 1дин 4: Салмагы / Көлөмү Формуласын Пайыз менен Эсептөө
 1 Аныктоо пайыз мазмун боюнча салмагы/ эритменин көлөмү. Проценттер эритменин жүз бөлүгүндө заттын канча бөлүгү бар экенин көрсөтөт. Химиялык эритмелерге колдонулганда, бул концентрация 1 пайызды түзсө, анда 100 миллилитр эритмеде 1 грамм зат бар, башкача айтканда 1 мл / 100 мл.
1 Аныктоо пайыз мазмун боюнча салмагы/ эритменин көлөмү. Проценттер эритменин жүз бөлүгүндө заттын канча бөлүгү бар экенин көрсөтөт. Химиялык эритмелерге колдонулганда, бул концентрация 1 пайызды түзсө, анда 100 миллилитр эритмеде 1 грамм зат бар, башкача айтканда 1 мл / 100 мл. - Мисалы, салмагы боюнча: 10% салмактагы эритмеде 100 миллилитр эритмеде ээриген 10 грамм зат бар.
- Мисалы, көлөмү боюнча: көлөмү боюнча 23 пайыздык эритменин ар бир 100 миллилитр эритмесинде 23 миллилитр суюк кошулма бар.
 2 Даярдагыңыз келген чечимдин көлөмүн аныктаңыз. Заттын керектүү массасын билүү үчүн, адегенде сизге керектүү болгон эритменин акыркы көлөмүн аныкташыңыз керек. Бул көлөм сизге канча чечим керек, канча жолу колдоносуз жана даяр чечимдин туруктуулугуна жараша болот.
2 Даярдагыңыз келген чечимдин көлөмүн аныктаңыз. Заттын керектүү массасын билүү үчүн, адегенде сизге керектүү болгон эритменин акыркы көлөмүн аныкташыңыз керек. Бул көлөм сизге канча чечим керек, канча жолу колдоносуз жана даяр чечимдин туруктуулугуна жараша болот. - Эгерде сиз ар дайым жаңы чечимди колдонушуңуз керек болсо, бир колдонууга керектүү сумманы гана даярдаңыз.
- Эгерде чечим узак убакыт бою өзүнүн касиеттерин сактап калса, кийинчерээк колдонуу үчүн чоңураак сумманы даярдай аласыз.
- Мисал: 500 мл көлөмдөгү 5% NaCl эритмесин даярдоо керек.
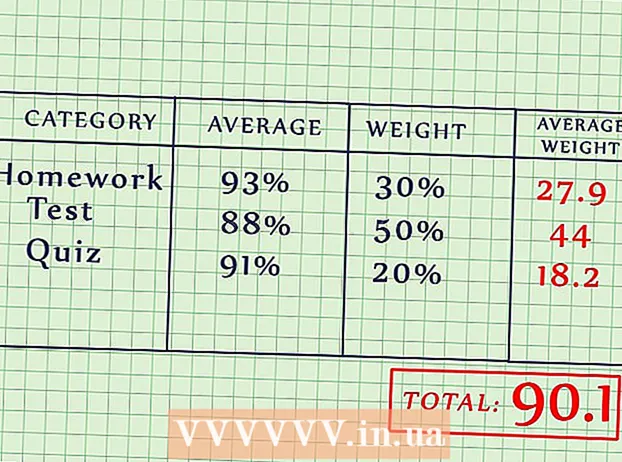
 3 Эритмени даярдоо үчүн керек болгон заттын граммынын санын эсептөө. Граммдын керектүү санын эсептөө үчүн төмөнкү формуланы колдонуңуз: граммдын саны = (пайыз талап кылынат) (керектүү көлөм / 100 мл). Мында керектүү пайыздар грамм менен, ал эми керектүү көлөм миллилитр менен көрсөтүлөт.
3 Эритмени даярдоо үчүн керек болгон заттын граммынын санын эсептөө. Граммдын керектүү санын эсептөө үчүн төмөнкү формуланы колдонуңуз: граммдын саны = (пайыз талап кылынат) (керектүү көлөм / 100 мл). Мында керектүү пайыздар грамм менен, ал эми керектүү көлөм миллилитр менен көрсөтүлөт. - Мисал: 500 мл көлөмдөгү 5% NaCl эритмесин даярдоо керек.
- грамм саны = (5г) (500мл / 100мл) = 25 грамм.
- Эгерде NaCl эритме катары берилсе, анда грамм порошоктун ордуна 25 миллилитр NaCl алып, акыркы көлөмдөн 25 миллилитр NaClден 475 миллилитр сууга алып салыңыз.
 4 Затты таразалаңыз. Заттын керектүү массасын эсептеп чыккандан кийин, бул сумманы өлчөөңүз керек. Калибрленген таразаны алыңыз, үстүнө идишти коюп, нөлдү коюңуз. Заттын керектүү өлчөмүн грамм менен таразалап, төгүп салыңыз.
4 Затты таразалаңыз. Заттын керектүү массасын эсептеп чыккандан кийин, бул сумманы өлчөөңүз керек. Калибрленген таразаны алыңыз, үстүнө идишти коюп, нөлдү коюңуз. Заттын керектүү өлчөмүн грамм менен таразалап, төгүп салыңыз. - Эритмени даярдоону улантуудан мурун, таразанын идишин порошоктун калдыктарынан тазалоону унутпаңыз.
- Жогорудагы мисалда сиз 25 грамм NaCl таразалашыңыз керек.
 5 Затты керектүү өлчөмдөгү суюктукта эритүү. Башкача каралбаса, суу ээритүүчү катары колдонулат. Өлчөөчү стаканды алып, керектүү өлчөмдөгү суюктукту ченеп алыңыз. Андан кийин порошок материалын суюктукта эритип алыңыз.
5 Затты керектүү өлчөмдөгү суюктукта эритүү. Башкача каралбаса, суу ээритүүчү катары колдонулат. Өлчөөчү стаканды алып, керектүү өлчөмдөгү суюктукту ченеп алыңыз. Андан кийин порошок материалын суюктукта эритип алыңыз. - Чечимди сактай турган контейнерге кол коюңуз. Затты жана анын концентрациясын так көрсөтүңүз.
- Мисалы: 25 грамм NaClди 500 миллилитр сууда эритип, 5% эритме жасаңыз.
- Эсиңизде болсун, эгер сиз суюк затты суюлтуп жатсаңыз, керектүү сууну алуу үчүн, кошулган заттын көлөмүн эритменин акыркы көлөмүнөн алып салыңыз: 500 мл - 25 мл = 475 мл суу.
Метод 2 4: Молекулярдык эритмени даярдоо
 1 Формуланы колдонуу менен колдонулган заттын молекулярдык салмагын аныктаңыз. Бирикменин формуласынын салмагы (же жөн эле молекулярдык салмагы) бөтөлкөнүн дубалына бир молге грамм (г / моль) менен жазылат. Эгер бөтөлкөдөгү молекулярдык салмагын таба албасаңыз, интернеттен караңыз.
1 Формуланы колдонуу менен колдонулган заттын молекулярдык салмагын аныктаңыз. Бирикменин формуласынын салмагы (же жөн эле молекулярдык салмагы) бөтөлкөнүн дубалына бир молге грамм (г / моль) менен жазылат. Эгер бөтөлкөдөгү молекулярдык салмагын таба албасаңыз, интернеттен караңыз. - Заттын молекулярдык салмагы - ошол заттын бир молунун массасы (грамм менен).
- Мисал: натрий хлоридинин (NaCl) молекулярдык салмагы 58,44 г / моль.
 2 Литр керектүү эритменин көлөмүн аныктоо. Бир литр эритмени даярдоо өтө оңой, анткени анын молярдуулугу моль / литр менен көрсөтүлөт, бирок эритменин максатына жараша көбүрөөк же азыраак литрди жасоо керек болушу мүмкүн. Керектүү граммды эсептөө үчүн акыркы көлөмдү колдонуңуз.
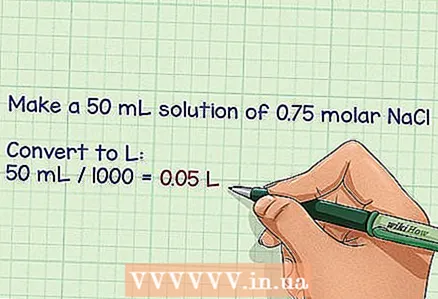
2 Литр керектүү эритменин көлөмүн аныктоо. Бир литр эритмени даярдоо өтө оңой, анткени анын молярдуулугу моль / литр менен көрсөтүлөт, бирок эритменин максатына жараша көбүрөөк же азыраак литрди жасоо керек болушу мүмкүн. Керектүү граммды эсептөө үчүн акыркы көлөмдү колдонуңуз. - Мисалы: NaCl молярдык бөлүгү 0,75 болгон 50 мл эритмени даярдоо керек.
- Милилитрди литрге айландыруу үчүн, аларды 1000ге бөлүп, 0,05 литр алыңыз.
 3 Керектүү молекулярдык эритмени даярдоо үчүн канча грамм керек экенин эсептеңиз. Бул үчүн төмөнкү формуланы колдонуңуз: граммдын саны = (керектүү көлөм) (керектүү молярдык) (формулага ылайык молекулярдык салмагы). Эсиңизде болсун, керектүү көлөм литр менен, molarity литрге моль менен, ал эми формула боюнча молекулярдык салмагы молге грамм менен.
3 Керектүү молекулярдык эритмени даярдоо үчүн канча грамм керек экенин эсептеңиз. Бул үчүн төмөнкү формуланы колдонуңуз: граммдын саны = (керектүү көлөм) (керектүү молярдык) (формулага ылайык молекулярдык салмагы). Эсиңизде болсун, керектүү көлөм литр менен, molarity литрге моль менен, ал эми формула боюнча молекулярдык салмагы молге грамм менен. - Мисалы: 50 мл NaCl 0,75 молярдык үлүшү бар эритмени даярдагыңыз келсе (формулага ылайык молекулярдык салмагы: 58.44 г / моль), сиз NaCl граммынын санын эсептешиңиз керек.
- граммдын саны = 0,05 л * 0,75 моль / л * 58,44 г / моль = 2,19 грамм NaCl.
- Өлчөө бирдиктерин азайтуу менен, сиз грамм зат аласыз.
 4 Затты таразалаңыз. Туура калибрленген балансты колдонуу менен керектүү сумманы таразалаңыз. Таразага таразага бир табакты коюп, нөл коюңуз. Каалаган массага жеткенче идишке затты кошуңуз.
4 Затты таразалаңыз. Туура калибрленген балансты колдонуу менен керектүү сумманы таразалаңыз. Таразага таразага бир табакты коюп, нөл коюңуз. Каалаган массага жеткенче идишке затты кошуңуз. - Таразаны колдонгондон кийин тазалаңыз.
- Мисалы: 2.19 грамм NaCl салмагы.
 5 Порошокту керектүү өлчөмдөгү суюктукта эритип алыңыз. Башкача айтылбаса, көпчүлүк чечимдер сууну колдонушат. Бул учурда, заттын массасын эсептөө үчүн колдонулган суюктуктун ошол эле көлөмү алынат. Сууга затты кошуп, толугу менен ээригенче аралаштырыңыз.
5 Порошокту керектүү өлчөмдөгү суюктукта эритип алыңыз. Башкача айтылбаса, көпчүлүк чечимдер сууну колдонушат. Бул учурда, заттын массасын эсептөө үчүн колдонулган суюктуктун ошол эле көлөмү алынат. Сууга затты кошуп, толугу менен ээригенче аралаштырыңыз. - Эритмеси бар контейнерге кол коюңуз. Чечимди кийинчерээк колдонуу үчүн эриген жана молярдыкты так белгилеңиз.
- Мисал: Стакандын жардамы менен (көлөмүн өлчөөчү прибор) 50 мл сууну өлчөп, ичинде 2.19 грамм NaCl ээрит.
- Чачты порошок толугу менен эригенче аралаштырыңыз.
Метод 3 3: Белгилүү концентрациядагы эритмелерди суюлтуу
 1 Ар бир эритменин концентрациясын аныктаңыз. Эритмелерди суюлтканда, сиз баштапкы эритменин концентрациясын жана алууну каалаган эритмени билишиңиз керек.Бул ыкма концентрацияланган эритмелерди суюлтууга ылайыктуу.
1 Ар бир эритменин концентрациясын аныктаңыз. Эритмелерди суюлтканда, сиз баштапкы эритменин концентрациясын жана алууну каалаган эритмени билишиңиз керек.Бул ыкма концентрацияланган эритмелерди суюлтууга ылайыктуу. - Мисал: 5 М эритмеден 75 миллилитр 1,5 М NaCl эритмесин даярдаңыз. Запастагы эритме 5 М концентрацияга ээ жана аны 1,5 М концентрацияга чейин суюлтуу керек.
 2 Акыркы чечимдин көлөмүн аныктаңыз. Алууну каалаган чечимдин көлөмүн табуу керек. Бул эритмени керектүү концентрацияга жана көлөмгө чейин суюлтуу үчүн керектүү болгон эритменин суммасын эсептеп чыгууга туура келет.
2 Акыркы чечимдин көлөмүн аныктаңыз. Алууну каалаган чечимдин көлөмүн табуу керек. Бул эритмени керектүү концентрацияга жана көлөмгө чейин суюлтуу үчүн керектүү болгон эритменин суммасын эсептеп чыгууга туура келет. - Мисал: Баштапкы 5 М эритмеден 75 миллилитр 1,5 М NaCl эритмесин даярдаңыз.Бул мисалда акыркы чечимдин көлөмү 75 миллилитр.
 3 Баштоочу эритмени суюлтуу үчүн керектүү эритменин көлөмүн эсептеңиз. Бул үчүн төмөнкү формула керек: V1C1= V2C2кайда В.1 - керектүү эритменин көлөмү, С.1 - анын концентрациясы, В.2 - акыркы чечимдин көлөмү, C.2 - анын концентрациясы.
3 Баштоочу эритмени суюлтуу үчүн керектүү эритменин көлөмүн эсептеңиз. Бул үчүн төмөнкү формула керек: V1C1= V2C2кайда В.1 - керектүү эритменин көлөмү, С.1 - анын концентрациясы, В.2 - акыркы чечимдин көлөмү, C.2 - анын концентрациясы. - Керектүү суюктуктун көлөмүн эсептөө үчүн Vге карата теңдикти кайра жазуу керек1: V1 = (В.2C2) / C.1.
- Мисал: 5 М концентрациядагы эритмеден 1,5 М концентрациядагы 75 мл NaCl эритмесин даярдоо керек.
- В.1 = (В.2C2) / C.1 = (0,075 л * 1,5 М) / 5М = 0,0225 л.
- Литрди кайра миллилитрге айландырып, 22,5 миллилитр алуу үчүн 1000ге көбөйтүңүз.
 4 Пландаштырылган акыркы көлөмдөн баштапкы чечимдин көлөмүн алып салыңыз. Эритмени суюлтуунун натыйжасында белгиленген акыркы көлөмдү алуу зарыл. Суюлтулган эритменин көлөмүн аныктоо үчүн акыркы көлөмдөн акциянын эритмесинин көлөмүн алып салыңыз.
4 Пландаштырылган акыркы көлөмдөн баштапкы чечимдин көлөмүн алып салыңыз. Эритмени суюлтуунун натыйжасында белгиленген акыркы көлөмдү алуу зарыл. Суюлтулган эритменин көлөмүн аныктоо үчүн акыркы көлөмдөн акциянын эритмесинин көлөмүн алып салыңыз. - Мисалы: Акыркы көлөмү 75 миллилитр жана баштапкы көлөмү 22,5 миллилитр. Ошентип, биз 75 - 22,5 = 52,5 миллилитрди алабыз. Дал ушул көлөмдөгү суюктук эритмени суюлтуу үчүн керек болот.
 5 Сток эритмесинин эсептелген суммасын суюлтуу суюктугу менен аралаштырыңыз. Стаканды (суюктуктун көлөмүн өлчөөчү прибор) колдонуп, кампанын эритмесинин керектүү өлчөмүн ченеп, суюлтуучу суюктуктун керектүү көлөмү менен аралаштырыңыз.
5 Сток эритмесинин эсептелген суммасын суюлтуу суюктугу менен аралаштырыңыз. Стаканды (суюктуктун көлөмүн өлчөөчү прибор) колдонуп, кампанын эритмесинин керектүү өлчөмүн ченеп, суюлтуучу суюктуктун керектүү көлөмү менен аралаштырыңыз. - Мисал: 5 М NaCl эритмесинин 22.5 миллилитрин өлчөп, 52.5 миллилитр суу менен суюлтуу. Чечимди аралаштырыңыз.
- Суюлтулган эритмеси бар идишке анын концентрациясын жана курамын жазыңыз: 1,5 М NaCl.
- Унутпаңыз, эгер кислотаны суу менен суюлтуп жатсаңыз, сууга кислота кошушуңуз керек, бирок эч качан тескерисинче.
Метод 4 4: Коопсуздук чараларын сактоо
 1 Жеке коргонуу шаймандарын колдонуңуз. Агрессивдүү химиялык заттар жана эритмелер менен иштегенде, алардын таасиринен коргоңуз. Лабораториялык пальто, жабык бут кийим, коргоочу көз айнек жана кол кап кийүүнү унутпаңыз.
1 Жеке коргонуу шаймандарын колдонуңуз. Агрессивдүү химиялык заттар жана эритмелер менен иштегенде, алардын таасиринен коргоңуз. Лабораториялык пальто, жабык бут кийим, коргоочу көз айнек жана кол кап кийүүнү унутпаңыз. - Күйүүчү эмес материалдан жасалган лабораториялык пальто колдонуңуз.
- Коопсуздук көз айнектеринин каптал калканчтары болушу керек, алар капталдан көздү жаап турат.
 2 Жакшы желдетилген жерде иштеңиз. Эритмелер аралашканда учуучу газдар бөлүнүп чыгышы мүмкүн. Кээ бир заттар лабораториялык капот астында гана иштетилиши керек. Эгерде сиз үйдө чечимдерди аралаштырып жатсаңыз, терезелерди ачыңыз жана желдеткичти күйгүзүңүз.
2 Жакшы желдетилген жерде иштеңиз. Эритмелер аралашканда учуучу газдар бөлүнүп чыгышы мүмкүн. Кээ бир заттар лабораториялык капот астында гана иштетилиши керек. Эгерде сиз үйдө чечимдерди аралаштырып жатсаңыз, терезелерди ачыңыз жана желдеткичти күйгүзүңүз.  3 Сууга кислота кошуу. Концентрацияланган кислоталарды суюлтканда дайыма кислотаны сууга кошуп коюңуз. Суу менен кислотаны аралаштырганда экзотермикалык (жылуулуктун бөлүнүшү менен) реакция пайда болот, бул кислотага суу кошулса жарылууга алып келиши мүмкүн, тескерисинче.
3 Сууга кислота кошуу. Концентрацияланган кислоталарды суюлтканда дайыма кислотаны сууга кошуп коюңуз. Суу менен кислотаны аралаштырганда экзотермикалык (жылуулуктун бөлүнүшү менен) реакция пайда болот, бул кислотага суу кошулса жарылууга алып келиши мүмкүн, тескерисинче. - Кислоталар менен иштеген сайын коопсуздук чараларын унутпаңыз.
Кеңештер
- Баштоодон мурун тема менен таанышып алыңыз. Билим - бул күч!
- Кадимки үй буюмдарын колдонууга аракет кылыңыз. Өзгөчө бир нерсе кылууга аракет кылбаңыз. Эгерде сиз коркунуч пайда болушу мүмкүн деп шектенсеңиз, багыныңыз.
Эскертүүлөр
- Агартуучу менен аммиакты аралаштырбаңыз.
- Коопсуздук жабдууларын, көз айнекти, пластикалык алжапкычты жана неопрен кол каптарын керектүү учурда колдонуңуз.
Сага эмне керек
- Массасын аныктоо үчүн так механикалык же электрондук таразалар. Мисалы, ашкана таразасын колдонсоңуз болот.
- Бүтүрүүчү айнек идиштер. Бул идиштерди ашкана дүкөнүнөн тапса болот же интернеттен заказ кылса болот. Өлчөөчү айнек түрдүү формада жана өлчөмдө болот. Пластикалык идиштер иштейт, бирок алар жогорку температурага туруштук бере албайт.